Оглавление:
Закон периодичности
ПЕРИОДИЧЕСКИЙ ЗАКОН
Д. И. МЕНДЕЛЕЕВА
«Свойства элементов, а потому и образуемых ими простых и сложных тел (веществ), стоят в периодической зависимости от их атомного веса».
«свойства химических элементов (т.е. свойства и форма образуемых ими соединений) находятся в периодической зависимости от заряда ядра атомов химических элементов».
Физический смысл химической периодичности
Периодические изменения свойств химических элементов обусловлены правильным повторением электронной конфигурации внешнего энергетического уровня (валентных электронов) их атомов с увеличением заряда ядра.
Графическим изображением периодического закона является периодическая таблица. Она содержит 7 периодов и 8 групп.
Период — горизонтальные ряды элементов с одинаковым максимальным значением главного квантового числа валентных электронов.
Номер периода обозначает число энергетических уровней в атоме элемента.
Периоды могут состоять из 2 (первый), 8 (второй и третий), 18 (четвертый и пятый) или 32 (шестой) элементов, в зависимости от количества электронов на внешнем энергетическом уровне. Последний, седьмой период незавершен.
Все периоды (кроме первого) начинаются щелочным металлом ( s -элементом), а заканчиваются благородным газом ( ns 2 np 6 ).
Металлические свойства рассматриваются, как способность атомов элементов легко отдавать электроны, а неметаллические — присоединять электроны из-за стремления атомов приобрести устойчивую конфигурацию с заполненными подуровнями. Заполнение внешнего s — подуровня указывает на металлические свойства атома, а формирование внешнего p — подуровня — на неметаллические свойства. Увеличение числа электронов на p — подуровне (от 1 до 5) усиливает неметаллические свойства атома. Атомы с полностью сформированной, энергетически устойчивой конфигурацией внешнего электронного слоя ( ns 2 np 6 ) химически инертны.
В больших периодах переход свойств от активного металла к благородному газу происходит более плавно, чем в малых периодах, т.к. происходит формирование внутреннего ( n — 1) d — подуровня при сохранении внешнего ns 2 — слоя. Большие периоды состоят из четных и нечетных рядов.
У элементов четных рядов на внешнем слое ns 2 — электроны, поэтому преобладают металлические свойства и их ослабление с ростом заряда ядра невелико; в нечетных рядах формируется np — подуровень, что объясняет значительное ослабление металлических свойств.
Группы — вертикальные столбцы элементов с одинаковым числом валентных электронов, равным номеру группы. Различают главные и побочные подгруппы.
Главные подгруппы состоят из элементов малых и больших периодов, валентные электроны которых расположены на внешних ns — и np — подуровнях.
Побочные подгруппы состоят из элементов только больших периодов. Их валентные электроны находятся на внешнем ns — подуровне и внутреннем ( n — 1) d — подуровне (или ( n — 2) f — подуровне).
В зависимости от того, какой подуровень ( s -, p -, d — или f -) заполняется валентными электронами, элементы периодической системы подразделяются на: s — элементы (элементы главной подгруппы I и II групп), p — элементы (элементы главных подгрупп III — VII групп), d — элементы (элементы побочных подгрупп), f — элементы (лантаноиды, актиноиды).
В главных подгруппах сверху вниз металлические свойства усиливаются, а неметаллические ослабевают. Элементы главных и побочных групп сильно отличаются по свойствам.
Номер группы показывает высшую валентность элемента (кроме O , F , элементов подгруппы меди и восьмой группы).
Общими для элементов главных и побочных подгрупп являются формулы высших оксидов (и их гидратов). У высших оксидов и их гидратов элементов I — III групп (кроме бора) преобладают основные свойства, с IV по VIII — кислотные.
school-sector.relarn.ru
Закон периодичности в психическом развитии ребенка (Д.Б. Эльконин).
Д.Б.Эльконин развил представления Л.С. Выготского о возрастном развитии. Он рассматривает ребенка как целостную личность, активно познающую окружающий мир — мир предметов и человеческих отношений, включая его при этом в две системы отношений: «ребенок — вещь» и «ребенок — взрослый». Но вещь, обладая определенными физическими свойствами, заключает в себе и общественно выработанные способы действий с нею. Это по сути — общественный предмет, действовать с которым ребенок должен научиться. Взрослый тоже не только человек, имеющий конкретные индивидуальные качества, но и представитель какой-то профессии, носитель других видов общественной деятельности с их специфическими задачами и мотивами, нормами отношений, т.е. общественный взрослый. Деятельность ребенка внутри систем «ребенок — общественный предмет» и «ребенок — общественный взрослый» представляет единый процесс, в котором формируется его личность.
В то же время эти системы отношений осваиваются ребенком в деятельностях разного типа. Среди видов ведущей деятельности, оказывающей наиболее сильное влияние на развитие ребенка, Д.Б.Эльконин выделяет две группы.
В первую группу входят деятельности, которые ориентируют ребенка на нормы отношений между людьми. Это непосредственно-эмоциональное общение младенца, ролевая игра дошкольника и интимно-личностное общение подростка. Они значительно отличаются друг от друга по содержанию и глубине, но представляют собой деятельности одного типа, имеющие дело главным образом с системой отношений «ребенок — общественный взрослый», или, шире, «человек — человек».
Вторую группу составляют ведущие деятельности, благодаря которым усваиваются общественно выработанные способы действий с предметами и различные эталоны: предметно-манипулятивная деятельность ребенка раннего возраста,
учебная деятельность младшего школьника и учебно-профессиональная деятельность старшеклассника. Маленький ребенок овладевает предметными действиями с ложкой или стаканом, ребенок старшего возраста — математикой и грамматикой, их деятельность мало похожа внешне, но по существу, и то и другое — освоение элементов человеческой культуры. Деятельности второго типа имеют дело с системой отношений «ребенок — общественный предмет» или «человек — вещь».
В деятельности первого типа главным образом развивается мотивационно-потребностная сфера, в деятельности второго типа формируются операционно-технические возможности ребенка, т.е. интеллектуально-познавательная сфера. Эти две линии образуют единый процесс развития личности, но на каждом возрастном этапе получает преимущественное развитие одна из них. Так как ребенок поочередно осваивает системы отношений «человек — человек» и «человек — вещь», происходит закономерное чередование и сфер, наиболее интенсивно развивающихся: в младенчестве развитие мотивационной сферы опережает развитие сферы интеллектуальной, в следующем, раннем возрасте мотивационная сфера отстает и более быстрыми темпами развивается интеллект и т.д.
Д.Б.Эльконин так формулирует закон периодичности:
«К каждой точке своего развития ребенок подходит с известным расхождением между тем, что он усвоил из системы отношений человек — человек, и тем, что он усвоил из системы отношений человек — предмет. Как раз моменты, когда это расхождение принимает наибольшую величину, и называются кризисами, после которых идет развитие той стороны, которая отставала в предшествующий период. Но каждая из сторон подготавливает развитие другой».
Таким образом, каждый возраст характеризуется своей социальной ситуацией развития; ведущей деятельностью, в которой преимущественно развивается мотивационно-потребностная или интеллектуальная сфера личности; возрастными новообразованиями, формирующимися в конце периода, среди них выделяется центральное, наиболее значимое для последующего развития. Границами возрастов служат кризисы — переломные моменты в развитии ребенка.
agespsyh.ru
Периодический закон Менделеева
Главный закон, управляющий миром химических элементов, открыл великий русский ученый Дмитрий Иванович Менделеев.
Ко времени этого открытия было известно 63 химических элемента. Накопилось огромное количество сведений и об их свойствах. Однако, изобилие не осмысленных с единой точки зрения фактов было источником трудностей и путаницы в химии. Гениальный русский химик, открыв закон, которому подчиняются свойства элементов, а также и строение атомов, разрешил эти трудности.

Дмитрий Иванович Менделеев.
Тщательно изучая и сопоставляя свойства химических элементов, он стремился раскрыть тайны далекого и близкого их родства.
Менделеев так описывает, свои искания: «. невольно зарождается мысль о том, что между массой и химическими особенностями элементов необходимо должна быть Связь. Искать же что-либо — хотя бы грибов или какую-либо зависимость — нельзя иначе, как смотря и пробуя. Вот я и стал подбирать, написав на отдельных карточках элементы с их атомными весами и коренными свойствами, сходные элементы и близкие атомные веса, что быстро и привело к тому заключению, что свойства элементов стоят в периодической зависимости от их атомного веса. »
Расположив элементы в порядке нарастания атомных весов, ученый получил ряды элементов; в каждом из рядов свойства элементов периодически повторяются.
По определению самого Менделеева, открытый им периодический закон заключается в том, что «свойства элементов (а следовательно, и образованных ими простых и сложных тел) находятся в периодической зависимости от их атомных весов».
Великую прозорливость проявил Менделеев, открыв периодичность в мире элементов, в то время когда множество элементов не было еще открыто, а атомные веса некоторых из известных элементов были определены неверно. Но доказать неопровержимо существование этой закономерности оказалось делом чрезвычайно трудным.
Когда Менделеев в своих изысканиях исходил из атомных весов, встречавшихся в работах того времени, периодичность нередко нарушалась.
Но ученый не стал в тупик. Он твердо был убежден в существовании периодической зависимости свойств элементов от их атомных весов. И когда он наблюдал нарушения периодичности, для него был возможен лишь один-единственный вывод, — очевидно, неверны или неполны данные, которыми располагала наука. Он исправлял на основании теоретических расчетов атомные веса некоторых элементов. Так было с индием, платиновыми металлами, ураном и другими элементами; позднейшие, более точные измерения их весов подтвердили правильность этих исправлений.
В 1869 году, опубликовав в журнале Русского химического общества свою работу «Соотношение свойств с атомным весом элементов», Менделеев познакомил ученый мир с открытым им периодическим законом. К статье была приложена таблица периодической системы элементов. Излагая сущность открытого закона, великий ученый указывал также на существование еще неизвестных науке элементов.
В таблице Менделеева химические элементы располагаются в порядке возрастания их атомного веса.
Много мест в своей системе Менделеев оставил для еще не открытых элементов, примерный атомный вес и другие свойства которых ученый высчитал, учитывая характер соседних элементов. Менделеев впервые в истории химии предсказал существование неизвестных элементов. Он писал, что должны существовать еще элементы, которые он назвал экаалюминием, экабором и экакремнием.
Ряд ученых отнесся к предсказанию русского ученого с большим недоверием.
Но вот в августе 1875 года французский ученый Лекок де Буа-бодран путем спектрального анализа обнаружил в цинковой обманке новый элемент, названный им галлием (Галлия — старинное наименование Франции).
В 1879 году известный шведский химик Нильсон открыл второй из предсказанных Менделеевым элементов. Свойства скандий, как назвал новый элемент Нильсон, полностью совпали со свойствами предсказанного Менделеевым экабора. Оправдались даже опасения русского ученого, что открытию экабора в минералах будет мешать присутствие другого химического элемента — иттрия.
«Таким образом, — заканчивает Нильсон свое сообщение об открытии нового элемента, — подтверждаются соображения русского химика, которые не только позволили предсказать существование названных элементов — скандия и галлия, но и предвидеть заранее их важнейшие свойства».
Наконец в 1886 году немецкий ученый Винклер открыл третий предугаданный Менделеевым элемент. В своем сообщении об этом Винклер указывал, что новый элемент — германий — как раз и есть предсказанный Менделеевым экакремний.
Это было полное торжество открытия Менделеева.
Фридрих Энгельс писал, что открытием периодического закона Менделеев «совершил научный подвиг».
Открытие Менделеева явилось могучим подтверждением одного из основных законов диалектики — закона перехода количества в качество.
Свойства химических элементов зависят от атомных весов. Закон перехода количества в качество, как писал Фридрих Энгельс, «имеет силу. и для самих химических элементов».
Одним из укрепителей периодического закона Д. И. Менделеева был известный чешский ученый Богуслав Браунер (1855—1935). Браунер своими работами подтвердил, что место, указанное Менделеевым для химического элемента бериллия в системе, является правильным. Отсюда и атомный вес этого элемента, высчитанный русским ученым на основании периодического закона, тоже правилен.
Менделеев с благодарностью писал потом о работе Б. Ф. Браунера, вспоминая, как часто ему «приходилось слышать о том, что вопрос об атомном весе бериллия грозит поколебать общность периодического закона, может потребовать глубоких в нем преобразований».
Атомный вес церия Менделеев исправил на основании открытого им закона с 92, как было признано всеми, на 138. Это вызвало бурный протест со стороны некоторых ученых.
«Как, — писал химик Раммельсберг, — исправлять атомные веса, руководствуясь какой-то таблицей! Да это чистейшей воды спекуляция!— шумел он. — Это подгон фактов под какую-то схему!»
Менделеев ответил на это: «Я полагаю, что ныне не должно, невозможно делать какие-либо точные соображения об элементах, минуя закон периодичности».
Позднее Браунер своими работами подтвердил правильность атомного веса церия, теоретически выведенного Менделеевым. Браунер же, а затем и английский физик Мозли указали на необходимость выделения в особое место так называемых редкоземельных элементов.
В 1884 году ученый-революционер Н. А. Морозов, находясь в заключении в Шлиссельбургской крепости, закончил там свою работу по анализу таблицы Менделеева. Он тоже теоретически предсказал существование группы химических элементов — инертных газов.

Принадлежность элемента к той или иной группе таблицы Менделеева указывает на количество протонов и нейтронов в ядре атома элемента и количество электронов в электронной оболочке.

Принадлежность элемента к тому или иному периоду таблицы Менделеева говорит о количестве слоев в электронной оболочке атома.
Там, где теперь в таблице Менделеева поставлены «благородные газы» — гелий, неон, аргон и другие, у Морозова были числа 4, 20, 40 и т. д., показывающие атомные веса недостающих элементов. Все эти химические элементы были выделены Морозовым в отдельную, нулевую группу.
Предвидение русских ученых было подтверждено работами английских ученых Релея и Рамзея, открывших инертные газы.
Неоспоримо величие русского гения — Менделеева. Но все же нашлись люди, которые пытались отнять у Менделеева право называться автором периодического закона. Менделеев вступил в борьбу за приоритет России в открытии периодического закона.
«Утверждение закона, — писал он, — возможно только при помощи вывода из него следствий, без него невозможных и неожидаемых, и оправдания тех следствий в опытной проверке. Потому-то, увидев периодический закон, я со своей стороны (1869—1871 гг.) вывел из него такие логические следствия, которые могли показать, верен ли он или нет. Без такого способа испытания не может утвердиться ни один закон природы. Ни Шанкуртуа, которому французы приписывают право на открытие периодического закона, ни Ньюлендс, которого выставляют англичане, ни Л. Мейер, которого цитировали иные как основателя периодического закона, не рисковали предугадывать свойства неоткрытых элементов, изменять «принятые веса атомов» и вообще считать периодический закон новым, строго постановленным законом природы, могущим охватывать еще доселе необобщенные факты, как это сделано мною с самого начала».
Предвосхищая позднейшие открытия естествознания, гениальный творец периодического закона предсказал, что атом неделим лишь химическим способом.
С помощью закона Менделеева русские ученые Б. Н. Чичерин и Н. А. Морозов (об их работах говорится ниже) предложили на основании умозрительных положений первую модель атома, в которой он изображается в виде системы тел, напоминающей солнечную систему. Позднейшие опытные исследования и математические расчеты показали, что такое уподобление имеет некоторые основания.
Закон Менделеева — мощное орудие познания природы и ее закономерностей. Все последующее развитие химии и физики шло в непосредственной связи с законом Менделеева и в зависимости от него. Все открытия в этих науках освещались его законом. С помощью этого закона показывался теоретический смысл открытий. В то же время каждое такое открытие приводило к уточнению и расширению закона, не затрагивая его принципиальных основ.
Руководствуясь периодическим законом, наука определила строение атомов всех элементов, которые, как установлено, состоят из электронной оболочки и ядра.
Число электронов возрастает от одного у атома водорода до 101 у атома менделеевия, открытого недавно и названного именем первооткрывателя периодического закона; число это находится в полном соответствии с порядковым номером элемента в системе Менделеева. Заряд ядра равен сумме зарядов электронов. Положительный заряд ядра, уравновешивающий отрицательные электроны, растет от 1 до 101. Положительный заряд ядра — это основное свойство атома, сообщающее ему химическую индивидуальность, так как от положительного заряда ядра зависит число электронов.
Ядро также оказалось сложным: оно состоит из протонов и нейтронов. Это основная масса атома; масса электрона в расчет не принимается, так как она в 1836,5 раза меньше массы протона.
Электроны у всех атомов одинаковы, но располагаются они вокруг ядра в различных слоях. Количество этих слоев раскрывает глубочайшее значение периодов, на которые разбиты все элементы в системе Менделеева. Каждый период отличается от другого наличием у атомов его элементов лишнего электронного слоя.
От строения электронной оболочки зависят химические свойства атома, так как химические реакции связаны с обменом внешних электронов. Кроме того, ряд физических свойств — электро- и теплопроводность, а также и оптические свойства тоже связаны с электронами.
Современная наука все шире и шире раскрывает значение гениального творения Менделеева.
Периодический закон указывал на сходство химических свойств элементов, расположенных в одной группе, то есть в одном и том же вертикальном столбце таблицы.
Теперь это прекрасно объясняется строением электронной оболочки атома. Элементы одной и той же группы имеют одинаковое количество электронов во внешнем слое: элементы первой группы — литий, натрий, калий и другие — имеют по одному электрону во внешнем слое; элементы второй группы — бериллий, магний, кальций и другие — по два электрона; элементы третьей группы — по три, и, наконец, элементы нулевой группы: гелий — два, неон, криптон и другие — по восемь электронов. Это максимальное из возможных количество электронов в наружном слое и обеспечивает данным атомам полную инертность: в обычных условиях они не вступают в химические соединения.

Изотопы.
Современная наука показала, что вес атомов одного и того же элемента может быть не одинаков, — это зависит от различного количества нейтронов в атомном ядре данного химического элемента. Поэтому в отдельной клетке менделеевской таблицы располагается не один тип атомов, а несколько. Такие атомы называются изотопами (в переводе с греческого «изотоп» означает «занимающий одно и то же место»). Химический элемент олово состоит, например, из 12 разновидностей, чрезвычайно близких по свойствам, но с разными атомными весами: средний атомный вес олова 118,7.
Изотопы имеются почти у всех элементов.
Пока обнаружено 300 естественных изотопов, искусственно удалось получить около 800. Но все они закономерно располагаются в 101 клетке таблицы Менделеева.
Все эти открытия, вызванные к жизни законом Менделеева, подчеркивают гениальность русского ученого, открывшего основной закон неживой природы, который, однако, имеет также колоссальное значение и для органического мира.
Системой Менделеева пользуются сейчас ученые и при расщеплении атомов и при создании новых элементов.
Этим атомным законом руководствуются и химики, и физики, и геологи, и агрономы, и строители, и механики, и электрики, и астрономы.
Спектроскоп показал, что элементы, которые существуют на Земле, есть и на других планетах. Те химические превращения, какие происходят у нас, могут протекать и в других частях вселенной.
Современная наука вторглась в недра атома. Родилась новая наука — физика атомного ядра. Воздействуя на атомное ядро, ученые теперь превращают одни элементы в другие, синтезируют такие элементы, которых в земной коре в настоящее время не встречается. К новым, искусственно созданным элементам относится группа заурановых химических элементов. Современная наука открыла путь и к использованию внутриядерной энергии. Все эти открытия неразрывно связаны с законом Менделеева.
www.stroitelstvo-new.ru
Справочник химика 21
Химия и химическая технология
Периодичности закон

ПЕРИОДИЧЕСКАЯ СИСТЕМА ЭЛЕМЕНТОВ Д. И. МЕНДЕЛЕЕВА — естественная система химических элементов, созданная гениальным русским химиком Д. И. Менделеевым. Расположив элементы в последовательности возрастания атомных масс и сгруппировав элементы с аналогичными свойствами, Д. И. Менделеев составил таблицу элементов, закономерности которой теоретически вытекают из сформулированного им периодического закона Физические и химические свойства элементов, проявляющиеся в свойствах простых и сложных тел, ими образуемых, находятся в периодической зависимости от их атомного веса (1869—1871 гг.). Периодический закон и периодическая система элементов Д. И. Менделеева позволяют установить свя ь между всеми химическими элементами, предсказать существование ранее неизвестных элементов и описать их свойства. Как впоследствии стало известно, периодичность в изменении свойств элементов обусловлена числом электронов в атоме, электронной структурой атома, периодически изменяющейся по мере возрастания числа электронов. Число электронов равно положительному заряду атомного ядра это число равно порядковому (атомному) номеру элемента в периодической системе элементов Д. И. Менделеева. Отсюда современная формулировка периодического закона Свойства элементов, а также свойства образованных ими простых и сложных соединений находятся в периодической зависимости от величины зарядов их атомных ядер (2) . Поскольку атомные массы элементов, как правило, возрастают в той же последовательности, что и заряды атомных ядер, современная форма таблицы периодической системы элементов полностью совпадает с менделеевской, где аргон, кобальт, теллур расположены не в порядке возрастания атомной массы, а на основе их химических свойств. Это несоответствие рассматривалось противниками Д. И. Менделеева как недостаток его системы, но, как позже было доказано, закономерность нарушается в связи с изотопным составом элементов, что также предвидел Д. И. Менделеев. Периодический закон и периодическая система элементов [c.188]
Согласно формулировке закона Д. И. Менделеева периодичность изменения свойств касается не только химических элементов, но и образуемых ими простых и сложных веществ. Периодичность изменения обнаружена для молярных объемов, температур плавления и кипения, для магнитных и электрических свойств, для теплот образования, теплоемкости и многих других физико-химических свойств, характеризующих простые и сложные вещества. [c.22]
Объяснение физического смысла Периодического закона представляет собой одно из важнейших достижений квантовой механики в химии. Для понимания природы периодичности необходимо иметь в виду следующее [c.100]
I См. также Закон периодичности (стр. 41). [c.281]
ДИАЛЕКТИКА ПЕРИОДИЧНОГО ЗАКОНА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ. [c.310]
Как же складывались у Менделеева формулировки основных понятий учения о периодичности закона периодичности и перио- [c.230]
Эта формулировка наводит на ответ столб воздуха должен быть электропроводным при разряде молнии и должен быть неэлектропроводным в остальное время. Разряд молнии сравнительно редкое явление, к тому же очень быстро проходящее. Закон согласования ритмики периодичность появления молниеотвода должна быть та же, что и периодичность появления молнии. [c.196]
Периодический закон периодичность свойств элементов. Периодический закон бы/ открыт Д. И. Менделеевым в 1869 г. и сформулирован им следующим образом свойства простых тел, такл Библиография для Периодичности закон: [c.184] Смотреть страницы где упоминается термин Периодичности закон: [c.150] [c.325] [c.41] [c.2] [c.5] [c.78] [c.19] [c.425] [c.83] [c.22] Справочник Химия изд.2 (2000) — [ c.100 ]
chem21.info
Периодический закон Д. И. Менделеева и периодическая система химических элементов
Периодический закон Д.И. Менделеева и периодическая система химических элементов имеет большое значение в развитии химии. Окунемся в 1871 год, когда профессор химии Д.И. Менделеев, методом многочисленных проб и ошибок, пришел к выводу, что «… свойства элементов, а потому и свойства образуемых ими простых и сложных тел, стоят в периодической зависимости от их атомного веса». Периодичность изменения свойств элементов возникает вследствие периодического повторения электронной конфигурации внешнего электронного слоя с увеличением заряда ядра.
Современная формулировка периодического закона такова:
«свойства химических элементов (т.е. свойства и форма образуемых ими соединений) находятся в периодической зависимости от заряда ядра атомов химических элементов».
Преподавая химию, Менделеев понимал, что запоминание индивидуальных свойств каждого элемента, вызывает у студентов трудности. Он стал искать пути создания системного метода, чтобы облегчить запоминание свойств элементов. В результате появилась естественная таблица, позже она стала называться периодической.
Наша современная таблица очень похожа на менделеевскую. Рассмотрим ее подробнее.
Таблица Менделеева
Периодическая таблица Менделеева состоит из 8 групп и 7 периодов.
Вертикальные столбцы таблицы называют группами. Элементы, внутри каждой группы, обладают сходными химическими и физическими свойствами. Это объясняется тем, что элементы одной группы имеют сходные электронные конфигурации внешнего слоя, число электронов на котором равно номеру группы. При этом группа разделяется на главные и побочные подгруппы.
В Главные подгруппы входят элементы, у которых валентные электроны располагаются на внешних ns- и np- подуровнях. В Побочные подгруппы входят элементы, у которых валентные электроны располагаются на внешнем ns- подуровне и внутреннем (n — 1) d- подуровне (или (n — 2) f- подуровне).
Все элементы в периодической таблице, в зависимости от того, на каком подуровне (s-, p-, d- или f-) находятся валентные электроны классифицируются на: s- элементы (элементы главной подгруппы I и II групп), p- элементы (элементы главных подгрупп III — VII групп), d- элементы (элементы побочных подгрупп), f- элементы (лантаноиды, актиноиды).
Высшая валентность элемента (за исключением O, F, элементов подгруппы меди и восьмой группы) равна номеру группы, в которой он находится.
Для элементов главных и побочных подгрупп одинаковыми являются формулы высших оксидов (и их гидратов). В главных подгруппах состав водородных соединений являются одинаковыми, для элементов, находящихся в этой группе. Твердые гидриды образуют элементы главных подгрупп I — III групп, а IV — VII групп образуют а газообразные водородные соединения. Водородные соединения типа ЭН4 – нейтральнее соединения, ЭН3 – основания, Н2Э и НЭ — кислоты.
Горизонтальные ряды таблицы называют периодами. Элементы в периодах отличаются между собой, но общее у них то, что последние электроны находятся на одном энергетическом уровне (главное квантовое число n — одинаково).
Первый период отличается от других тем, что там находятся всего 2 элемента: водород H и гелий He.
Во втором периоде находятся 8 элементов (Li — Ne). Литий Li – щелочной металл начинает период, а замыкает его благородный газ неон Ne.
В третьем периоде, также как и во втором находятся 8 элементов (Na — Ar). Начинает период щелочной металл натрий Na, а замыкает его благородный газ аргон Ar.
В четвёртом периоде находятся 18 элементов (K — Kr) – Менделеев его обозначил как первый большой период. Начинается он также с щелочного металла Калий, а заканчивается инертным газом криптон Kr. В состав больших периодов входят переходные элементы (Sc — Zn) — d-элементы.
В пятом периоде, аналогично четвертому находятся 18 элементов (Rb — Xe) и структура его сходна с четвёртым. Начинается он также с щелочного металла рубидий Rb, а заканчивается инертным газом ксенон Xe. В состав больших периодов входят переходные элементы (Y — Cd) — d-элементы.
Шестой период состоит из 32 элементов (Cs — Rn). Кроме 10 d-элементов (La, Hf — Hg) в нем находится ряд из 14 f-элементов(лантаноиды)- Ce — Lu
Седьмой период не закончен. Он начинается с Франций Fr, можно предположить, что он будет содержать, также как и шестой период, 32 элемента. Но найдено пока только 24 (до элемента с Z = 110). Сюда входят 14 f-элементов, которые относятся к актиноидам.
Интерактивная таблица Менделеева
Если посмотреть на периодическую таблицу Менделеева и провести воображаемую черту, начинающуюся у бора и заканчивающуюся между полонием и астатом, то все металлы будут находиться слева от черты, а неметаллы – справа. Элементы, непосредственно прилегающие к этой линии будут обладать свойствами как металлов, так и неметаллов. Их называют металлоидами или полуметаллами. Это бор, кремний, германий, мышьяк, сурьма, теллур и полоний.
Периодический закон
Менделеев дал следующую формулировку Периодического закона: «свойства простых тел, а также формы и свойства соединений элементов, а потому и свойства образуемых ими простых и сложных тел, стоят в периодической зависимости от их атомного веса».
Существует четыре основных периодических закономерности:
Правило октета утверждает, что все элементы стремятся приобрести или потерять электрон, чтобы иметь восьмиэлектронную конфигурацию ближайшего благородного газа. Т.к. внешние s- и p-орбитали благородных газов полностью заполнены, то они являются самыми стабильными элементами.
Энергия ионизации – это количество энергии, необходимое для отрыва электрона от атома. Согласно правилу октета, при движении по периодической таблице слева направо для отрыва электрона требуется больше энергии. Поэтому элементы с левой стороны таблицы стремятся потерять электрон, а с правой стороны – его приобрести. Самая высокая энергия ионизации у инертных газов. Энергия ионизации уменьшается при движении вниз по группе, т.к. у электронов низких энергетических уровней есть способность отталкивать электроны с более высоких энергетических уровней. Это явление названо эффектом экранирования. Благодаря этому эффекту внешние электроны мене прочно связаны с ядром. Двигаясь по периоду энергия ионизации плавно увеличивается слева направо.
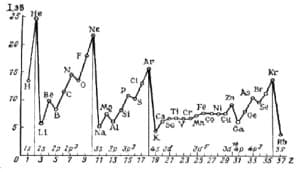 Зависимость энергии ионизации от заряда ядра
Зависимость энергии ионизации от заряда ядра
Сродство к электрону – изменение энергии при приобретении дополнительного электрона атомом вещества в газообразном состоянии. При движении по группе вниз сродство к электрону становится менее отрицательным вследствие эффекта экранирования.
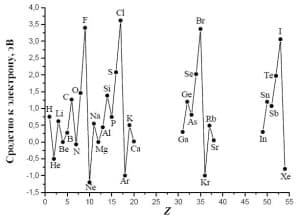 Зависимость сродства к электрону от заряда ядра
Зависимость сродства к электрону от заряда ядра
Электроотрицательность — мера того, насколько сильно атом стремится притягивать к себе электроны связанного с ним другого атома. Электроотрицательность увеличивается при движении в периодической таблице слева направо и снизу вверх. При этом надо помнить, что благородные газы не имеют электроотрицательности. Таким образом, самый электроотрицательный элемент – фтор.
 зависимость электроотрицательности от заряда ядра
зависимость электроотрицательности от заряда ядра
На основании этих понятий, рассмотрим как меняются свойства атомов и их соединений в таблице Менделеева.
Итак, в периодической зависимости находятся такие свойства атома, которые связанны с его электронной конфигурацией: атомный радиус, энергия ионизации, электроотрицательность.
Рассмотрим изменение свойств атомов и их соединений в зависимости от положения в периодической системе химических элементов.
Неметалличность атома увеличивается при движении в периодической таблице слева направо и снизу вверх. В связи с этим основные свойства оксидов уменьшаются, а кислотные свойства увеличиваются в том же порядке — при движении слева направо и снизу вверх. При этом кислотные свойства оксидов тем сильнее, чем больше степень окисления образующего его элемента
По периоду слева направо основные свойства гидроксидов ослабевают,по главным подгруппам сверху вниз сила оснований увеличивается. При этом, если металл может образовать несколько гидроксидов, то с увеличением степени окисления металла, основные свойства гидроксидов ослабевают.
По периоду слева направо увеличивается сила кислородосодержащих кислот. При движении сверху вниз в пределах одной группы сила кислородосодержащих кислот уменьшается. При этом сила кислоты увеличивается с увеличением степени окисления образующего кислоту элемента.
По периоду слева направо увеличивается сила бескислородных кислот. При движении сверху вниз в пределах одной группы сила бескислородных кислот увеличивается.
zadachi-po-khimii.ru
