АРОМАТИЧНОСТЬ
АРОМАТИЧНОСТЬ – сочетание определенных свойств, присущих большой группе соединений, называемых, соответственно, ароматическими.
Термин «ароматичность» ввел в 1865 Ф.Кекуле, установивший строение бензола и предложивший для него формулу:
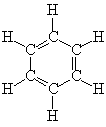

Название «ароматический» связано с тем, что среди производных бензола существуют соединения с приятным запахом (например, нитробензол имеет запах миндаля).
Кекуле обратил внимание на то, что двойные связи в бензоле и в его производных заметно отличаются по свойствам от двойных связей в большинстве ненасыщенных соединений. Для бензола оказались крайне затруднены реакции присоединения (например, галогенов) по двойным связям, которые в случае ненасыщенных соединений проходят достаточно легко.
Кроме того, обнаружилось, что орто-дихлорбензол (атомы хлора находятся у двух соседних атомов углерода) не имеет изомеров, которые можно было ожидать на основе предложенной для него структурной формулы, где два атома хлора расположены либо у простой, либо у двойной связи:
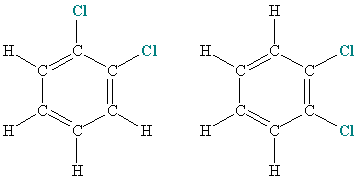
В результате Кекуле предложил назвать связи в бензоле осциллирующими, то есть колеблющимися. Со временем это предположение получило дальнейшее развитие, и было усовершенствовано.
Наиболее характерны для бензола реакции замещения атомов водорода. Изучение химии бензола показало, что замена атома водорода на какую-либо группу определенным и, главное, предсказуемым образом влияет на реакционную способность остальных атомов водорода.
Если в бензольное ядро ввести группу, оттягивающую электроны от ядра (например, метильную), то последующее галогенирование приводит к замещению в орто- и пара-положении. При введении электроноподающей группы (например, карбоксильной) галоген направляется в мета-положение:

Долгое время ароматичностью считали набор указанных химических свойств, но постепенно были найдены более точные признаки, основанные на особенностях строения ароматических соединений.
Электронное строение бензола и родственных ему соединений в современном понимании выглядит следующим образом. В образовании двойных связей участвуют р-электроны атомов углерода, орбитали (область наиболее вероятного расположения электрона в пространстве) этих электронов имеют форму объемных восьмерок. В случае бензола орбитали взаимоперекрываются, образуя кольцевые орбитали, на которых располагаются все р-электроны молекулы:

В результате появляется единая замкнутая электронная оболочка, система приобретает высокую стабильность. Фиксированные простые и двойные связи в бензоле отсутствуют, все связи С–С усреднены и эквивалентны, поэтому чаще для обозначения ароматичности используют кольцевой символ, помещенный внутри цикла:
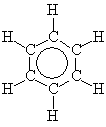
В образовавшихся циклических орбиталях возникает кольцевой ток, который может быть обнаружен специальными измерениями, дополнительно указывающими на ароматичность соединения.
Ароматичностью обладают плоские циклические молекулы, при этом количество электронов (m), объединенных в единую циклическую систему, должно соответствовать правилу Хюккеля:
m = 4n + 2 (n = 0, 1, 2, 3. ), n – число натурального ряда
Ниже показаны первые три представителя этого ряда ароматических молекул, соответствующие правилу Хюккеля: катион циклопропена 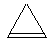 , бензол и нафталин.
, бензол и нафталин.
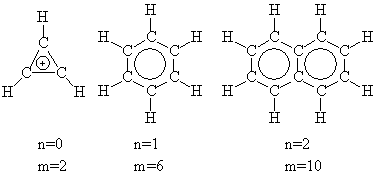
Расширение понятия «ароматичность» позволило применить этот термин к соединениям небензольного типа, но обладающим в то же время набором структурных и химических признаков, характерных для производных бензола.
В некоторых соединениях, где в состав цикла входят атомы O, S или N, например, в фуране, тиофене, пирроле так же, как в бензоле, существует устойчивая – в соответствии с правилом Хюккеля – шестиэлектронная замкнутая система. Четыре р-электрона (отмечены на рисунке синим цветом) предоставляют двойные связи цикла, а два s-электрона (отмечены красным цветом) дают атомы кислорода, серы или азота, имеющие неподеленную пару электронов.

Ароматическими могут быть не только плоские циклические молекулы, но и объемные структуры, например, сандвичевые молекулы (ферроцен, дибензолхром) и некоторые каркасные бороводороды:
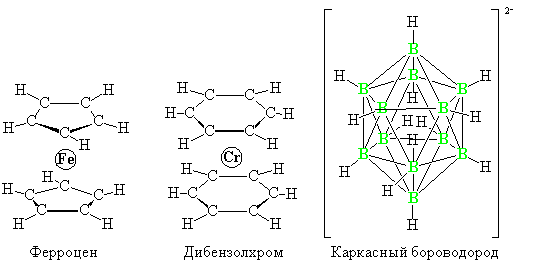
В случае объемных структур вместо правила Хюккеля применяют иные правила, определяющие то количество электронов, при котором возникает ароматичность. Однако, во всех этих случаях присутствуют основные признаки ароматичности: замкнутая электронная оболочка, высокая стабильность молекулы, склонность к реакциям замещения и влияние введенного заместителя на реакционную способность остальных реакционных центров в молекуле.
www.krugosvet.ru
Справочник химика 21
Химия и химическая технология
Ароматичность Хюккеля правило
Сформулируйте правило ароматичности Э. Хюккеля. Приведите примеры ароматических систем, отвечающих правилу Хюккеля, если 1) п=0, 2) п = 1, [c.142]
Ароматичность гетероциклов, правило Хюккеля. Основность и кислотность гетероциклов. Реакционная способность пиррола, пиридина, индола. Таутомерия а-окси- и а-аминопиридина, урацила, тимина, цитозина, аденина, гуанина. Водородные связи при ассоциациях гетероциклов, их окси- и аминопроизводных. Водородные связи в системах аденин — тимин, гуанин — цитозин. Понятие о ДНК и РНК, их биологическая роль. [c.191]
Однако к ароматичности ведет не только секстетная конфигурация л-электронов. Согласно правилу 4п + 2 Хюккеля относительно устойчивыми плоскими моноциклическими системами атомов с тригональной гибридизацией являются только системы, содержащие 4л -f 2 электронов. Это правило следует из простой теории МОХ, в которой для л-электронной циклической системы низшая связывающая орбиталь всегда заполняется двумя электронами, а все более высокие связывающие орбитали дважды вырождены и заполнены четырьмя электронами. Если число таких орбиталей п, то л-электрон-ная оболочка заполняется 4л + 2 электронами. Следовательно, ароматическими будут плоские моноциклические соединения, содержащие 2, 6, 10, 14 и т. д. л-электронов. Правило Хюккеля хорошо подтверждается на опыте. [c.119]
Хюккеля правило — один из признаков, определяющих ароматичность плоская циклическая структура является ароматической, если она содержит (4п + 2)п-электронов, участвующих в формировании единой делокализованной л-электронной системы. См. Бензол. [c.345]
ХЮККЕЛЯ ПРАВИЛО (правило ароматичности) циклические соед., молекулы к-рых состоят из атомов, вносящих н я-злектронную систему цикла 4и + 2 р-электропов ( = 0,1,2. ), обладают аром, св-вами. X. н. строго выполняется только для моноциклич. соед. Сформулировано [c.671]
Хюккель впервые применил метод молекулярных орбиталей и сформулировал правило ароматичности [138] относительно стабильны моноциклические плоские 5р -гибридизованные соединения с числом делокализованных я-электронов 4п + 2 (где п = О, 1, 2 И Т. д.). [c.236]
Структура и уст0йч1 Е0сть бензольного кольца. Ароматичность и правило Хюккеля. Изомерия и номенклатура производных бензола, [c.190]
Охарактеризуйте особенности строения соединений, проявляющих ароматичность. Сформулируйте правило Хюккеля. Какие из приведенных ниже соединений являются ароматическими [c.118]
Правило Хюккеля применимо для углеводородов с конденсированными (сочлененными) кольцами. Определите, какие соединения являются ароматическими объясните, почему антрацен и фенантрен менее ароматичны , чем бензол например, легко окисляются СгОз до хинонов. [c.120]
Все это связано с особенностью структур этих гетероциклических соединений. У них в пятичленных кольцах четыре л-электрона двух сопряженных двойных связей и неподеленная электронная пара гетероатома (О, 8, К) образуют секстет л-электронов, что укладывается в рамки правила ароматичности Хюккеля (4п-ь2) л-электронов в замкнутой системе сопряженных кратных связей (где п — целое неотрицательное число). Таким образом, эти шесть л-электронов кольца образуют делокализованную систему, как в бензоле [c.483]
Правило Хюккеля допускает существование ароматических систем, содержащих не только секстет электронов. Если в выражении 4и + 2 положить и = О, то окажется, что циклическая система, имеющая лишь два электрона, должна обладать свойствами ароматичности. Это — система циклопропенилия, ее синтезировал в 1957 г. Бреслау при взаимодействии толана с нитрилом диазофенилуксусной кислоты [c.80]
Следует подчеркнуть достоинство действия рассматриваемых правил, т. е. фактически обобщенной концепции ароматичности для циклических систем типа Хюккеля и Мебиуса. В отличие от метода корреляционных диаграмм, требующего наличия элементов симметрии для переходного состояния реакции, данный подход свободен от указанного ограничения. [c.508]
Эрих Хюккель (род. 1896 г.) — немецкий физик, большинство работ которого связано с решением химических проблем. Совместно с П. Дебаем и Л. Онзагером им разработана теория сильных электролитов (теория Дебая — Хюккеля). Ему принадлежит одна из наиболее плодотворных идей в теории строения сопряженных систем — идея а, я-приближения. Э. Хюккель сформулировал правило ароматичности Ап+2, предложил метод расчета я-электронных систем, носящий его имя. [c.212]
Мы говорили выше об эффективности простьк качественных концепций (типа стерических препятствий, индутсгивного эффекта, эффектов сольватации/десольватации и т.п.), повседневно применяемых в органической химии. Наиболее распространенные из них появились на свет как обобщения обширного эмпирического материала, накапливавшегося на протяжении десятилетий трудами поколений химиков всего мира. Квантовая. х]4мия способна на теоретической, неэ.мпирической основе порождать концепции такого же уровня простоты и удобства в применении. Выразительными примерами могут служить концепция ароматичности Хюккеля (правило 4л +2 ) и правила Вудворда—Хоффмана (сохранение орбитальной симметрии). Мы беремся утверждать, что вклад этих результатов в развитие органической химии несравненно более значителен, чем вклад всех достижений расчетных методов, вместе взятых. Их сила именно в простоте и общедоступности применения, в том, что они позволяют с единой точки зрения не только интерпретировать огромный фактический материал, но и уверенно предсказывать новые явления. Прийти к подобным концепциям на чисто эмпирической основе, а тем [c.547]
Аннулены — моноциклические углеводороды, содержащие сопряженные двойные связи и отвечающие общей формуле (СН), , где т > 2. Если цикл плоский, а т- нечетное число — 1, 3, 5 и т.д., тогда число л-электронов в единой сопряженной системе равно 4п + 2 (см. Ароматичность, Хюккеля правило) и молекула характеризуется ароматическими свойствами. [c.30]
Правило ароматичности Хюккеля (правило 4ш + 2). Ароматическими свойствами обладают все аннулены или их ионы с общим числом л-электронов, равным 4т + 2, где т = О, 1, 2, 3,. .. [c.352]
Особенности электронного строения ароматических соединений известны давно и нашли отражение в известном правиле ароматичности Хюккеля (1931—1933 гг.), которое в настоящее время формулируется следующим образом молекулы, включающие в основном состоянии набор орбиталей с участием Ап- -2п(р)-электронов, образующих замкнутый цикл, являются ароматическими. Позднее сформулировано аналогичное правило для антиароматических соединений (Бреслоу, 1959 г.) молекулы, включающие в основном состоянии набор орбиталей с участием Ап п(р)-электронов, образующих замкнутый цикл, являются антиаро-матическими. Естественно, что ароматические молекулы должны быть плоскими, иначе невозможно оёразование многоцентровой п-связи. В дальнейшем ароматические и антиароматические системы, отвечающие приведенным правилам, получили название хюккелевских систем. Следует отметить, что правила ароматиЧ ности и антиароматичности действительны не только для циклических полиенов, но и для циклических переходных состояний. [c.72]
Ароматичность, правило Хюккеля. Электрофильные и нуклеофильные реакции. Электронодонорность и электроноакценторность заместителей. Индуктивный эффект и эффект сопряжения. Теория замещения, ориентанты I и И рода. Реакции электрофильного и нуклеофильного замещения, реакции присоединения. Переходные состояния. Согласованная и несогласованная ориентация. Спектры (ПМР, ИК и УФ) ароматических соединений. [c.250]
Зная, что в атомах наряду с секстетом / -электронов существуют и другие устойчивые субоболочки — s , уместно спросить только ли секстет я-электронов ведет к ароматичности молекул Ответ на этот вопрос был дан Хюккелем, сформулировавшим правило 4п-ь2 относительно устойчивыми плоскими моноциклическими системами атомов с тригональной гибридизацией являются только системы, содержащие 4й+2 электронов, [c.232]
Правило (4и + 2) Хюккеля применимо и к макроциклическим четным полиенам, так называемым аннуленам. Так, ароматичны аннулены с [c.233]
По этому методу правила орбитальной симметрии связываются с правилом Хюккеля относительно ароматичности, которое обсуждалось в гл. 2. Правило Хюккеля, согласно которому циклическая электронная система, содержащая Ап- -2 электронов, является ароматической (а следовательно, стабильной), применимо, конечно, к молекулам в основных состояниях. При использовании принципа орбитальной симметрии мы имеем дело не с основным, а с переходным состоянием. В этом методе рассматриваются не сами молекулярные орбитали, а скорее р-орбитали до их перекрывания, приводящего к образованию молекулярных орбиталей. Такой набор р-орбиталей называется базисным набором (рис. 15.2). При рассмотрении возможности согласованной реакции орбитали базисного набора необходимо расположить в соответствии с положением, которое они займут в переходном состоянии. На рис. 15.3 это изображено для [2 + +2]- и [4-Ь2]-циклоирисоединения, Затем следует обратить внимание на обращение знака. Из рис. 15.3 очевидно, что ни в одном из случаев обращения знака не происходит. Пунктирная линия на этом рисунке соединяет только отрицательные доли орбиталей. Системы без обращения знака или с четным числом таких обращений называются системами Хюккеля. Системы с нечетным числом инверсий знака называются системами Мёбиуса (по аналогии с лентой Мёбиуса, которая представляет собой математическую поверхность, изображенную на рис. 15.4). Мёбиусовские системы не вступают ни в одну из этих реакций, а примеры таких систем приведены в т. 4 (см. описание реакций 18-31 и 18-36). [c.247]
Рассмотрение показывает. Что в таком случае происходит обращение правила Хюккеля, и длн 4пл-электронных систем предсказывается ароматичность. Поскольку пока не получена молекула, существующая в основном состоянии со скрученным сопряжением, это предсказание еще предстоит проверить. Однако его корректность подтверждается тем фактом, что переходные состояния с закрученным расгтоложеннем орбиталей, как оказалось, совершййно уместны при рассмотрении многих органических реакций [47]. Мы вернемся к зтому вопросу в следующей главе. Правила ароматичности можно обобщить, включив мёбиусовское расположение орбиталей [c.332]
Смотреть страницы где упоминается термин Ароматичность Хюккеля правило: [c.295] [c.234] [c.453] [c.453] [c.249] [c.151] [c.36] [c.180] [c.324] Органическая химия Том1 (2004) — [ c.387 ]
chem21.info
ХЮККЕЛЯ ПРАВИЛО
правило ароматичности: циклич. соед., молекулы к-рых состоят из атомов, вносящих в ПИ-электронную систему цикла 4n + 2 р-электронов (n = 0, 1, 2. ), обладают ароматич. свойствами. Строго выполняется только для моноциклич. соед. Правило сформулировано Э. Хюккелем в 1931.
Естествознание. Энциклопедический словарь .
Смотреть что такое «ХЮККЕЛЯ ПРАВИЛО» в других словарях:
ХЮККЕЛЯ МЕТОД — квантовохим. метод приближенного расчета энергетич. уровней и мол. орбиталей ненасыщенных орг. соединений. Основан на предположении, согласно к рому движение электрона вблизи атомного ядра в молекуле не зависит от состояний или числа др.… … Химическая энциклопедия
Ароматичность — Ароматичность особое свойство некоторых химических соединений, благодаря которому сопряженное кольцо ненасыщенных связей проявляет аномально высокую стабильность; большую чем та, которую можно было бы ожидать только при одном сопряжении.… … Википедия
АРОМАТИЧНОСТЬ — (от греч. aroma, род. падеж aromatos благовоние), понятие, характеризующее совокупность структурных, энергетич. св в и особенностей реакц. способности циклич. структур с системой сопряженных связей. Термин введен Ф. А. Кекуле (1865) для описания… … Химическая энциклопедия
Ароматические соединения — Запрос «Арены» перенаправляется сюда; см. также другие значения. Бензол одно из наиболее распространённых ароматических соединений Ароматические соединения циклические о … Википедия
p -ЭЛЕКТРОННОЕ ПРИБЛИЖЕНИЕ — квантовохим. метод изучения энергетич. состояний ненасыщенных соед., в к ром св ва молекулы соотносятся со строением системы орбита лей. В рамках молекулярных орбиталей методов все орбитали молекулы, ядерная конфигурация к рой имеет плоскость… … Химическая энциклопедия
ЭЛЕКТРОПРОВОДНОСТЬ ЭЛЕКТРОЛИТОВ — способность электролитов проводить электрич. ток при приложении электрич. напряжения. Носителями тока являются положительно и отрицательно заряженные ионы катионы и анионы, к рые существуют в р ре вследствие электролитич. диссоциации. Ионная Э. э … Химическая энциклопедия
Хюккель Эрих — (Нückel) (1896 1980), немецкий химик и физик. Основные труды в области квантово химических методов изучения строения молекул (правило Хюккеля и др.). Разработал (совместно с П. Дебаем, 1923) теорию сильных электролитов. * * * ХЮККЕЛЬ Эрих ХЮККЕЛЬ … Энциклопедический словарь
Хюккель, Эрих — Эрих Арманд Артур Йозеф Хюккель Erich Armand Arthur Joseph Hückel Эрих Хюккель (1938) … Википедия
Хюккель — Хюккель, Эрих Эрих Арманд Артур Йозеф Хюккель Erich Armand Arthur Joseph Hückel Эрих Хюккель (1938) Дата рождения: 9 августа … Википедия
Хюккель, Эрих Арманд Артур Йозеф — Эрих Хюккель (1938) Эрих Арманд Артур Йозеф Хюккель (нем. Erich Armand Arthur Joseph Hückel) (9 августа 1896, Берлин 16 февраля 1980, Марбург) немецкий физик и химик, один из основоположников квантовой химии, создатель теории сильных электролитов … Википедия
dic.academic.ru
Ароматичность
Ароматичность – понятие, характеризующее совокупность особых структурных, энергетических и магнитных свойств, а также особенностей реакционной способности циклических структур с системой сопряженных связей.
Хотя ароматичность – одна из важнейших и наиболее плодотворных концепций химии (не только органической), — не существует общепринятого краткого определения этого понятия. Ароматичность понимается через совокупность особых признаков (критериев), присущих ряду циклических сопряженных молекул в той или иной мере. Часть этих критериев имеет экспериментальную, наблюдаемую природу, но другая часть основывается на квантовой теории строения молекул. Ароматичность имеет квантовую природу. Невозможно объяснить ароматичность с позиций классической структурной теории и теории резонанса.
Не следует путать ароматичность с делокализацией и сопряжением. В молекулах полиенов (1,3-бутадиена, 1,3,5-гексатриена и т.п.) проявляется явно выраженная тенденция к делокализации электронов и образованию единой сопряженной электронной структуры, что проявляется в спектрах (в первую очередь, электронных спектрах поглощения), некотором изменении длин и порядков связей, энергетической стабилизации, особых химических свойствах (электрофильное 1,4-присоединение в случае диенов и пр.). Делокализация и сопряжение – необходимые, но не достаточные условия ароматичности. Можно дать определение ароматичности как свойства, при котором сопряженное кольцо ненасыщенных связей проявляет бόльшую стабильность, чем ту, которую можно было бы ожидать только при одном сопряжении. Однако этим определением нельзя пользоваться, не имея экспериментальных или расчётных данных по стабильности циклической сопряжённой молекулы.
Для того чтобы молекула могла быть ароматической, она должна содержать хотя бы один цикл, каждый из атомов которого располагает пригодной для образования ароматической системы р-орбиталью. Ароматическим в полном смысле этого слова считается (в случае выполнения критериев, перечисленных ниже) именно этот цикл (кольцо, система колец).
В этом цикле должно быть 4n+2 (то есть 2, 6, 10, 14, 18, 22 и т.п.) p-электронов.
Это правило называется правилом или критерием ароматичности Хюккеля. Источник этого правила – сильно упрощенные квантовохимические расчеты идеализированных циклических полиенов, произведенные на заре развития квантовой химии. Дальнейшие исследования показали, что в основе своей это простое правило дает верные предсказания ароматичности даже и для очень сложных реальных систем.
Правилом, тем не менее, нужно правильно пользоваться, иначе прогноз может быть неверен.
Какие орбитали считаются пригодными для образования ароматической системы? – Любые орбитали, перпендикулярные плоскости цикла, и
а) принадлежащие входящим в цикл кратным (эндоциклическим двойным или тройным) связям;
б) соответствующие неподеленным парам электронов у гетероатомов (азота, кислорода, и т.п.) или карбанионов;
в) соответствующие шестиэлектронным (секстетным) центрам, в частности карбокатионам.
Критерии ароматичности.
Энергетический (повышение термодинамической устойчивости за счет делокализации электронов, так называемая энергия делокализации – ЭД).

Можно представить бензол производным трёх молекул этилена и сравнить энергии исходных фрагментов и конечной молекулы. У каждой молекулы этилена по 2 p-электрона (всего 6) на молекулярных орбиталях (МО) одинаковой энергии (α+β), а у бензола 6 электронов располагаются на трёх связывающих молекулярных орбиталях, давая в сумме более отрицательное значение энергии системы (α и β меньше 0).
Очевидное энергетическое преимущество составляет 2β = 36 ккал/моль или 1,56 эВ – это ЭЭР (эмпирическая энергия резонанса).
Энергетический критерий из всех самый неудобный и неясный. Величины энергий для этого критерия берут всегда расчетные, потому что, как правило, невозможно подобрать соответствующую неароматическую молекулу для сравнения. Следует, поэтому, спокойно относиться к тому, что существует множество различных оценок энергии делокализации даже для классических ароматических молекул, а для более сложных систем эти величины вообще отсутствуют. Никогда нельзя сравнивать разные ароматические системы по величине энергий делокализации – нельзя сделать вывод, что молекула А ароматичнее молекулы В, потому что энергия делокализации больше.
Структурный – очень важный, если не самый важный, критерий, так как имеет не теоретическую, а экспериментальную природу. Специфика геометрии молекул ароматических соединений заключается в тенденции к копланарному расположению атомов и выравниванию длин связей. У бензола выравнивание длин связей идеально – все шесть С-С связей одинаковы по длине. У более сложных молекул выравнивание не идеально, но значительно. В качестве критерия берут меру относительного отклонения длин сопряженных связей от среднего значения. Чем ближе к нулю, тем лучше. Эту величину можно проанализировать всегда, если имеется структурная информация (экспериментальная или из высококачественного квантовохимического расчета). Тенденция к копланарности обуславливается выгодностью параллельного расположения осей атомных р-орбиталей для их эффективного перекрывания.
Магнитный (наличие кольцевого тока – диатропная система, влияние на химические сдвиги протонов снаружи и внутри кольца, примеры – бензол и [18]-аннулен). Самый удобный и доступный критерий, так как для его оценки достаточно спектра 1H ЯМР. Для точного определения используют теоретические расчеты химических сдвигов.
Химический – склонность к реакциям замещения, а не присоединения. Самый наглядный критерий, ясно различающий химию ароматических соединений от химии полиенов. Но работает он далеко не всегда. В ионных системах (например, в циклопентадиенил-анионе или тропилий-катионе) замещение наблюдать невозможно. Реакции замещения иногда проходят и на неароматических системах, а ароматические всегда в какой-то степени способны к реакциям присоединения. Поэтому химический критерий более правильно назвать признаком ароматичности.
Представление энергии ароматической системы.
Общая формула:
Ej(энергия орбитали j уровня) = α + mjβ
α – кулоновский интеграл, энергия С2р орбитали,
β – резонансный интеграл, энергия взаимодействия 2-х атомных орбиталей на соседних атомах
mj = 2сos(2jπ/N), где N- число атомов углерода в цикле.
Наиболее простым и наглядным графическим изображением энергии являтся круг Фроста. Для его построения необходимо вписать в окружность ароматическую молекулу, направив вершиной вниз, тогда точки соприкосновения многоугольника и окружности будут соответствовать энергетическим уровням МО. По вертикали наносится энергетическая шкала, все уровни ниже горизонтального диаметра – связывающие, выше – разрыхляющие. Электроны заполняют от самой нижней орбитали согласно правилу Паули.

Наиболее выгодным будет такое состояние, когда полностью заполнены все связывающие орбитали.
Попробуйте самостоятельно разобрать, почему является ароматичной молекула азулена, это не очень сложно, он является показательным примером. Нужно построить два круга Фроста (такие как для бензола выше) для обоих фрагментов молекулы: циклопентадиена и циклогептатриена – и станет очевидно, почему молекула приобретает полярность. Картинка-ответ за ссылкой рядом.
 Объяснение ароматичности Азулена с помощью круга Фроста
Объяснение ароматичности Азулена с помощью круга Фроста
Краткая история Бензола:
Открыт в 1825г. М. Фарадеем — выделен из светильной.
Кекуле размышлял о структуре бензола, и был вдохновлён обезьянами, что водили хоровод, это натолкнуло его на циклическую динамическую модель.


Позднее появилось ещё множество предположений о структуре бензола:

Однако даже до сих пор молекула C6H6 продолжает преподносить сюрпризы. Бодриков И.В.: «Я вынужден констатировать, что сейчас в мире нет человека, кто бы знал, что такое бензол» (2009)

(один из водородов перемещается в положение, перпендикулярное кольцу)
edu.tltsu.ru
Ароматичность: критерии ароматичности, правило ароматичности Хюккеля, примеры бензоидных и небензоидных ароматических соединений.
Циклические сопряженные системы представляют большой интерес как группа соединений с повышенной термодинамической устойчивостью по сравнению с сопряженными открытыми системами. Эти соединения обладают и другими особыми свойствами, совокупность которых объединяют общим понятием ароматичность. К ним относятся способность таких формально ненасыщенных соединений вступать в реакции замещения, а не присоединения, устойчивость к действию окислителей и температуры.
Типичными представителями ароматических систем являются арены и их производные. Особенности электронного строения ароматических углеводородов наглядно проявляются в атомно-орбитальной модели молекулы бензола. Каркас бензола образуют шесть sp 2 -гибридизованных атомов углерода. Все σ-связи (C-C и C-H) лежат в одной плоскости. Шесть негибридизованных р-АО расположены перпендикулярно плоскости молекулы и параллельно друг другу (рис. 3, а). Каждая р-АО в равной степени может перекрываться с двумя соседними р-АО. В результате такого перекрывания возникает единая делокализованная π-система, наибольшая электронная плотность в которой находится над и под плоскостью σ-скелета и охватывает все атомы углерода цикла (см. рис. 3, б). π-Электронная плотность равномерно распределена по всей циклической системе, что обозначается кружком или пунктиром внутри цикла (см. рис. 3, в). Все связи между атомами углерода в бензольном кольце имеют одинаковую длину (0,139 нм), промежуточную между длинами одинарной и двойной связей.
На основании квантовомеханических расчетов установлено, что для образования таких стабильных молекул плоская циклическая система должна содержать (4n + 2) π-электронов, где n = 1, 2, 3 и т. д. (правило Хюккеля, 1931). С учетом этих данных можно конкретизировать понятие «ароматичность».
Ароматические системы (молекулы)– системы, отвечающие критериям ароматичности:
1) наличие плоского σ-скелета, состоящего из sp 2 -гибридизованных атомов;
2) делокализация электронов, приводящая к образованию единого π-электрон-ного облака, охватывающего все атомы цикла (циклов);
3) соответствие правилу Э. Хюккеля, т.е. электронное облако должно насчитывать 4n+2 π-электронов, где n=1,2,3,4… (обычно цифра указывает на количество циклов в молекуле);
4) высокая степень термодинамической устойчивости (высокая энергия сопряжения).

Рис. 3.Атомно-орбитальная модель молекулы бензола (атомы водорода опущены; объяснение в тексте)

Устойчивость сопряженных систем.Образование сопряженной и особенно ароматической системы — энергетически выгодный процесс, так как при этом увеличивается степень перекрывания орбиталей и происходит делокализация (рассредоточение) р-электронов. В связи с этим сопряженные и ароматические системы обладают повышенной термодинамической устойчивостью. Они содержат меньший запас внутренней энергии и в основном состоянии занимают более низкий энергетический уровень по сравнению с несопряженными системами. По разнице этих уровней можно количественно оценить термодинамическую устойчивость сопряженного соединения, т. е. его энергию сопряжения(энергию делокализации). Для бутадиена-1,3 она невелика и составляет около 15 кДж/моль. С увеличением длины сопряженной цепи энергия сопряжения и соответственно термодинамическая устойчивость соединений возрастают. Энергия сопряжения для бензола гораздо больше и составляет 150 кДж/моль.
Примеры небензоидных ароматических соединений: 
Пиридинпо электронному строению напоминает бензол. Все атомы углерода и атом азота находятся в состоянии sp 2 -гибридизации, и все σ-связи (C-C, C-N и C-H) лежат в одной плоскости (рис. 4, а). Из трех гибридных орбиталей атома азота две участвуют в образовании

Рис. 4.Пиридиновый атом азота (а), распределение электронов по орбиталям (б) и сопряженная система в молекуле пиридина (в) (связи С-Н для упрощения рисунка опущены)
σ-связей с атомами углерода (показаны только оси этих орбиталей), а третья орбиталь содержит неподеленную пару электронов и в образовании связи не участвует. Атом азота с такой электронной конфигурацией называют пиридиновым.
За счет электрона, находящегося на негибридизованной р-орбитали (см. рис. 4, б), атом азота участвует в образовании единого электронного облака ср-электронами пяти атомов углерода (см. рис. 4, в). Таким образом, пиридин является π,π-сопряженной системой и удовлетворяет критериям ароматичности.
В результате большей электроотрицательности по сравнению с атомом углерода пиридиновый атом азота понижает электронную плотность на атомах углерода ароматического кольца, поэтому системы с пиридиновым атомом азота называют π-недостаточными. Кроме пиридина, примером таких систем служит пиримидин, содержащий два пиридиновых атома азота.
Пирролтакже относится к ароматическим соединениям. Атомы углерода и азота в нем, как и в пиридине, находятся в состоянии sp2-гибридизации. Однако в отличие от пиридина атом азота в пирроле имеет иную электронную конфигурацию (рис. 5, а, б).

Рис. 5.Пиррольный атом азота (а), распределение электронов по орбиталям (б) и сопряженная система в молекуле пиррола (в) (связи С-Н для упрощения рисунка опущены)
На негибридизованной р-орбитали атома азота находится неподеленная пара электронов. Она участвует в сопряжении с р-электрона- ми четырех атомов углерода с образованием единого шестиэлектронного облака (см. рис. 5, в). Три sp 2 -гибридные орбитали образуют три σ-связи — две с атомами углерода, одну с атомом водорода. Атом азота в таком электронном состоянии получил название пиррольного.
Шестиэлектронное облако в пирроле благодаря р,п-сопряжению делокализовано на пяти атомах цикла, поэтому пиррол представляет собой π-избыточную систему.
В фуранеи тиофенеароматический секстет также включает неподеленную пару электронов негибридизованной p-АО кислорода или серы соответственно. В имидазолеи пиразоледва атома азота вносят разный вклад в образование делокализованного электронного облака: пиррольный атом азота поставляет пару π-электронов, а пиридиновый — один p-электрон.

Ароматичностью обладает также пурин,представляющий собой конденсированную систему двух гетероциклов — пиримидина и имидазола.

Делокализованное электронное облако в пурине включает 8 π-электронов двойных связей и неподеленную пару электронов атома N=9. Общее число электронов в сопряжении, равное десяти, соответствует формуле Хюккеля (4n + 2, где п = 2).
Гетероциклические ароматические соединения обладают высокой термодинамической устойчивостью. Неудивительно, что именно они служат структурными единицами важнейших биополимеров — нуклеиновых кислот.
Дата добавления: 2015-05-26 ; просмотров: 14716 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
helpiks.org
