Выражения закона действующих масс для скорости прямой реакции
В 1865 г. профессор Н.Н. Бекетов впервые высказал гипотезу о количественной взаимосвязи между массами реагентов и временем течения реакции: «. притяжение пропорционально произведению действующих масс». Эта гипотеза нашла подтверждение в законе действующих масс, который был установлен в 1867 г. двуми норвежскими химиками К. Гульдбергом и П. Вааге. Современная формулировка закона действующих масс такова:
При постоянной температуре скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ, взятых в степенях, равных стехиометрическим коэффициентам в уравнении реакции.
Для реакции aA + bB → mM + nN математическое выражение закона действующих масс имеет вид:
где v — скорость реакции; k — коэффициент пропорциональности, называемый константой скорости химической реакции (при CA = CB = 1 моль/л k численно равна v); CA и CB — концентрации реагентов A и B; a и b — стехиометрические коэффициенты в уравнении реакции.
Константа скорости химической реакции k определяется природой реагирующих веществ и зависит от температуры, от присутствия катализатора, но не зависит от концентрации веществ, участвующих в реакции.
Закон действующих масс справедлив только для наиболее простых по своему механизму взаимодействий, протекающих в газах или в разбавленных растворах.
Часто уравнение реакции не отражает ее механизма. Сложные реакции могут быть совокупностью параллельно или последовательно протекающих процессов. Закон действующих масс справедлив для каждой отдельной стадии реакции, но не для всего взаимодействия в целом. Та стадия скорость которой минимальна, лимитирует скорость реакции в общем. Поэтому математическое выражение закона действующих масс, записанное для самой медленной (лимитирующей) стадии процесса, приложимо одновременно ко всей реакции в целом.
Примеры решения задач:
Задача 1. Во сколько раз изменится скорость прямой и обратной реакций в системе 2SO2(г) + O2 = 2SO3(г) , если объем газовой смеси уменьшить в 3 раза? В какую сторону сместится равновесие системы?
Решение. Обозначим концентрации реагирующих веществ CSO2 = a, CO2 = b, CSO3 = d. Согласно закону действующих масс, скорости прямой и обратной реакций до изменения объема:
После уменьшения объема гомогенной системы в 3 раза концентрация каждого из реагирующих веществ увеличится в 3 раза: CSO2 = 3a, CO2 = 3b, CSO3 = 3d. При новых концентрациях скорости прямой и обратной реакций:
v’прямая = k1 · (3a) 2 · 3b = 27 · k1 · a 2 · b;
Изменения скоростей составят:
Следовательно, скорость прямой реакции увеличилась в 27 раз, а обратной — в 9 раз. Равновесие системы сместилось в сторону образования SO3.
Источники информации:
- Коровин Н.В., Масленникова Г.Н., Мингулина Э.И., Филиппов Э.Л. Курс общей химии. — М.: Высшая школа, 1990. — С. 109-110, 140-141
Если вы нашли ошибку на странице, выделите ее и нажмите Ctrl + Enter.
© Сбор и оформление информации: Кипер Руслан
chemister.ru
Справочник химика 21
Химия и химическая технология
Гульдберг закон действия масс
В курсе общей химии рассматривается вывод уравнения константы равновесия кинетическим путем—на основе равенства скоростей прямой и обратной реакций и зависимости скорости реакции от концентрации реагирующих веществ. Таким же путем закон действия масс был выведен Гульдбергом и Вааге (1867). Однако этот путь можно применить лищь для сравнительно простых реакций. В общем же случае следует использовать термодинамический вывод. [c.259]
Этим правилом и определяется влияние концентрации на скорость реакции. Оно было выражено (в несколько иной форме) впервые Гульдбергом и Вааге (1867). Его также называют законом действия масс, как и закон, выражающий константу равновесия реакции, ибо, как мы увидим в 197, оба они тесно связаны между собой. Для газовых реакций это правило является строгим только в пределах применимости законов идеальных газов. Оно применимо также и к реакциям в разбавленных растворах (строго только для бесконечно разбавленных растворов). В математической форме в применении, например, к реакции [c.465]
Закон действия масс Гульдберга и Вааге дал бы химикам, изучающим обратимые реакции, значительно больше, чем гипотеза Бертло, которая к тому же, как мы уже говорили, оказалась не совсем верной, но, к сожалению, Гульдберг и Вааге сначала (1867 г.) опубликовали свою работу на норвежском языке, и она оставалась незамеченной, пока ее в 1879 г. не перевели на немецкий язык . [c.112]
При заданных внешних условиях (Т, Р, среда, Ю) скоросчь является функцией копцентрации реагирующих веществ. Основной постулат химической кинетики (закон действующих масс, Гульдберг и Вааге) определяет, что скорость реакции, протекающей в статических условиях, пр0110р1ДИ011альна произведению концентрации реагирующих веществ в с гспенях, равных их стехиометрическим коэффициентам в уравнении реакции [c.137]
Ч Закон действующих масс. О степени протекания процесса можно судить на основании закона действующих масс, которому подчиняется система в состоянии равновесия частное от деления произведения равновесных концентраций продуктов реакции на произведение равновесных концентраций исходных веществ является величиной по стоянной (Гульдберг и Вааге, 1864—1867). Эту величину называют константой равновесия, ее обозначают К. [c.178]
Закон действия масс. Основным законом химической кинетики является открытый в 1864—1867 гг. Гульдбергом и Вааге (Норвегия) закон действия масс, согласно которому скорость элементарной реакции пропорциональна произведению концентраций реагирующих веществ в степенях, равных стехиометрнческим коэффициентам. Такая зависимость скорости реакции от концентрации обусловлена тем, что вероятность столкновения молекул и, следовательно, нх взаимодействия, пропорциональна произведению концентраций реагентов. [c.214]
Зависимость скорости элементарной реакции от концентрации реагирующих веществ выражает, как известно, закон действующих масс (Гульдберг и Вааге). В соответствии с этим законом, i.opo Tb химической реакции пропорциональна концентрациям [c.20]
Согласно закону действия масс, скорость химической реакции пропорциональна активным массам реагентов. Этот закон был впервые установлен на основании результатов экспериментальных наблюдений Гульдбергом и Вааге в 1864—1867 гг. (см., например, литературу ), а затем теоретически обоснован на базе теории молекулярных столкновений в жидкостях и газах. В первоначальной трактовке под активной массой понимали концентрацию в единицах массы на единицу объема, но время от времени высказывались и другие интерпретации данного термина. Так, например, Аррениус предполагал, что осмотическое давление, а Вант-Гофф считал, что растворимость, так же как и концентрация, связаны с активной массой. [c.22]
Для фиксированных начальных условий Т , Р скорость реакции пропорциональна концентрации компонентов. Эта зависимость впервые была сформулирована Гульдбергом и Вааге в виде так называемого закона действия масс (или закона действующих масс — ЗДМ), который для простой реакции (элементарной стадии) можно записать в виде [c.15]
Скорость элементарной реакции равна произведению концентраций реагентов, участвующих в химическом акп1е, возведенных в степени, равные стехиометрическим коэффициентам реакции. Уравнение (195.1) является основным законом кинетики. Коэффициенты v могут принимать только целые положительные значения, равные 1, 2, 3. Закон действующих масс был впервые сформулирован Гульдбергом и Вааге (1867). Пфаундлер уравнение (195.1) теоретически вывел на базе молекулярно-кинетической теории (1867). Часто односторонние реакции могут протекать через стадии образования промежуточных соединений реагирующих молекул с молекулами растворителя или катализатора, с последующим превращением в продукты реакции. Тогда уравнение скорости химической реакции записывают в форме [c.533]
Уравнения (34.5) и (34.6) являются аналитическим выражением закона действия масс (ЗДМ), который был впервые выведен Гульдбергом и Вааге из кинетических соображений. Константы равновесия Кр и К связаны соотношением [c.166]
В эту переломную эпоху перехода от фактов, ждущих своего объяснения, к теоретическим выводам в совершенно новой и мало понятной области химии—катализе—большие услуги оказала физическая химия, устанавливающая закономерности на основе каталитических реакций. В 1870 г. Л. Вильгельми открыл кинетический закон действия масс при каталитическом исследовании инверсии тростникового сахара под действием разбавленных кислот. Это позволило позднее в 1867 г. К. Гульдбергу и П. Вааге сформулировать общий закон действия масс в виде динамического равновесия. К этому времени относятся классические исследования Я. Вант-Гоффа по законам кинетики (принципы различия моно-, ди- и по-лимолекулярных реакций), работы М. Боденштейна по газовым реакциям и их кинетике и исследования В. Оствальда по катализу. [c.18]
В 1867 г. норвежские ученые К. Гульдберг (1836—1902) и П. Вааге (1833— 1900) на основании изучения трудов Бертолле и тщательной экспериментальной проверки их достоверности предложили первое математическое описание влияния концентрации реагирующих веществ на выход продуктов реакции. Выводы, полученные ими, в окончательной форме в 1877 г. были высказаны голландским физико-химиком Я. X. Вант-Гоффом и общепризнаны под наименованием закона действия масс. [c.131]
Указанная закономерность называется законом действующих масс (Гульдберг и Вааге). [c.212]
Условие равновесия для системы, где происходит химическая реакция, выведено нами в связи с рассмотрением общей термодинамической теории равновесия [формула (1Х.32)]. Из условия (1Х.32) легко получить основной закон химического равновесия— закон действия масс, если химические потенциалы в явной форме выразить через концентрации или парциальные давления компонентов. Впервые закон действия масс был сформулирован норвежскими учеными Гульдбергом и Вааге (1867) на основе кинетического рассмотрения идеальных газов. [c.240]
Полученное соотношение выражает закон действия масс для химической реакции, протекающей при столкновении двух частиц (К. Гульдберг и П. Вааге, 1867 г) [c.194]
Математик М. Гульдберг и химик П. Вааге показали, что законы химического равновесия могут быть выведены математически из кинетического закона действия, масс и привели экспериментальные доказательства этому. [c.343]
В 1867 г. после работ Н. И. Бекетова шведскими учеными К. Гульдбергом и П. Вааге был сформулирован закон действия масс. Впоследствии Я. Вант-Гоффом было разработано математическое выражение кинетических закономерностей, Н. А. Меншуткиным (1887) исследована кинетика химических реакцин в растворах и выяснена роль растворителя С. Аррениусом разработана теория электролитической диссоциации (1887) и исследовано влияние температуры на скорость химических реакций (1889). [c.7]
Задачей физической химии, а точнее термохимии и термодинамики, и является определение тепловых эффектов химических реакций, их зависимости от условий и в первую очередь от температуры. Изучение тепловых явлений, сопровождающих химические реакции, а также некоторых термических свойств реагирующих веществ, а именно их энтропий и теплоемкостей, позволяет установить общие критерии самопроизвольного течения реакции, а также критерии равновесия. При этом в результате некоторых приближений можно вывести один из важных законов химии — закон действующих масс, открытый на основании иных предположений норвежскими учеными Гульдбергом и Вааге (1867). Суть дела можно свести к возможности теоретического вычисления константы равновесия (Кр) и определению [c.5]
Выражение (У. 116) является одной из форм закона действующих масс, выведенного иным путем в 1867 г. Гульдбергом и Вааге. [c.135]
В этом заключается основное содержание закона действующих масс, установленного К. Гульдбергом и П. Вааге (1867) и получившего строгую физико-химическую интерпретацию в работах Я. Вант-Гоффа (1885), который решил задачу о максимальной работе химической реакции Ащах, совершаемую системой при переходе от произвольных концентраций Гг (или давлений р,) к равновесным концентрациям С, (или давлениям р,) [c.33]
Закон действующих масс был выведен Гульдбергом и Вааге из статистических соображений. [c.49]
Первая попытка установить связь между скоростью реакций и концентрацией реагентов была сделана Н. Н. Бекетовым (1865). Более строго эту закономерность установили в 1867 г. скандинавские ученые химик Гульдберг и математик Вааге. Закон действия масс — соотношение, лежащее в основе химической кинетики. Он строго выполняется только для гомогенных реакций, протекающих в разбавленных растворах, или при взаимодействии газов, близких к идеальным, т. е. находящихся под низким давлением. [c.138]
В результате работ Н. И. Бекетова (1865 г.), математика Гульдберга и химика Вааге (1867 г.) нашла подтверждение мысль о том, что химическое действие зависит от концентрации взаимодействующих веществ. Был установлен закон действия масс, и тем самым идеи Бертолле были облечены в математическую форму — обратимость химической реакции получила количественное выражение. [c.380]
Эта зависимость была впервые сформулирована в прошлом веке Гульдбергом и Вааге и известна в физической химии как закон действия масс. [c.174]
Равновесие в обратимых химических реакциях описывается законом действующих масс (з. д. м.) (Гульдберг, Вааге, 1867). Если концентрации или парциальные давления веществ — участников реакции сравнительно малы, то з. д. м. устанавливает постоянство отно-шения произведения равновесных концентраций (или парциальных давлений) продуктов реакции к произведению концентраций (или парциальных давлений) исходных веществ, взятых в степенях, равных стехиометрическим коэффициентам (при Т = onst). [c.131]
Для развития атомно-молекулярного учения большую роль сыграли обобщающие закономерности, позволившие до создания учения о. статике и динамике процессов решить вопросы об энергетике процессов, скоростях их протекания, равновесии и влиянии на них внешних условий. К числу таких закономерностей следует отнести закон Гесса, закон действующих масс Гульдберга и Вааге и принцип Ле Шателье. [c.29]
Влияние концентрации веществ на скорость реакции определяется законом действующих масс, открытым К. Гульдбергом и П. Вааге (1864—1867), согласно которому при постоянной температуре скорость химической реакции пропорциональна произведению концентраций реагирующих веществ, возведенных в степенях, равных стехиометрическим коэффициентам в уравнении реакции. [c.20]
Закон действия масс был опытным путем установлен Бекетовым (1865 г.) и Гульдбергом и Вааге (1867 г.). [c.57]
Установлено, что скорость химической реакции прямо пропорциональна произведению молярных концентраций реагентов, если для реакции необходимо столкновение двух реагирующих молекул. Эта зависимость носит название закона действующих масс для скорости химической реакции (К. Гульдберг, П. Вааге, 1867 г.). Для реакции А 4- В -> Продукты этот закон выразится уравнением [c.28]
Полученное выражение носит название закона действующих масс для химического равновеси.ч (К. Гульдберг, П. Вааге, 1867 г.). [c.29]
Это уравнение называется уравнением константы молекулярного равновесия. Читается оно так отношение произведения молярных концентраций получившихся веществ к произведению молярных концентраций исходных веществ в момент подвижного равновесия есть величина постоянная (это есть фактическая формулировка закона действующих масс Гульдберга и Вооге). [c.162]
Константы Ki и Ка называются константами равновесия,. выраженными через фугитивности и активности. Выражения (VI. 16) и (VI. 17) по аналогии с уравнениями, выведенными Гульдбергом и Вааге в 1864 г. из представлений о равенстве скоростей реакции в состоянии равновесия, называют законом действующих масс. [c.367]
Основным законом, устанавливающим количественную зависимость между концентрациями продуктов реакции и исходных веществ в условиях равновесия, является закон действующих масс, выведенный Н. Гульдбергом и П. Вааге (1867) скорость химических реакций, протекающих в однородной среде, при постоянной температуре прямо пропорциональна произведению концентраций (активностей) реагирующих веществ, возведенных в степень их стехисметрических коэффициентов. [c.41]
Основываясь на этих представлениях и применяя выводы мо-лекулярногкинетической теории строения вещества, норвежские химики К- Гульдберг и П. Вааге в 1879 г. предложили общее выражение кинетич-еской формы закона действующих масс (ЗДМ) основанного на положении, что скорость реакции определяется вероятностью столкновения реагирующих частиц, т. е. пропорциональна их концентрации. [c.200]
Необходимо было выяснить их физический смысл. Первоначально пытались установить коэффициенты сродства для каждого соотношения взятых масс в отдельности. Затем возникла мысль найти общий путь вычисления условий равновесия для любых количеств реагирующих веществ. Широко используя как экспериментальные данные М. Бертло и Пеан де Сен-Жиля, так и собственные результаты, опираясь на принятое в 60-х годах XIX в. механистическое толкование природы сил сродства , К. Гульдберг и П. Вааге 2 в работах 1862—1867 гг. представили равновесие обратимой обменной реакции как равенство двух сил сродства, действующих в противоположных направлениях. Авторы математически сформулировали закон действующих масс они построили свою теорию на общем условии равновесия [c.326]
Смотреть страницы где упоминается термин Гульдберг закон действия масс: [c.247] [c.31] [c.132] [c.535] [c.247] [c.112] [c.115] [c.854] Физическая химия Том 1 Издание 4 (1935) — [ c.414 ]
chem21.info
Закон действующих масс

Пример оформления расчетной задачи
Задача 2. Вычислите степень диссоциации и равновесные концентрации ионов [OH — ] и [NH4 + ] в 0,1 М растворе гидроксида аммония, если К NH4OH =1,76∙10 -5 .
1. Записываем уравнение диссоциации гидроксида аммония, справа от уравнения приводим константу ионизации, во второй строке указываем начальные концентрации вещества, в третьей строке – равновесные концентрации всех частиц, в четвертой – убыль концентрации гидроксида аммония.
2. Составляем математическое выражение закона действующих масс, подставляем в него равновесные концентрации всех частиц и решаем относительно x.
 .
.Математически доказано, что если отношение
 , величиной x в знаменателе можно пренебречь.
, величиной x в знаменателе можно пренебречь.3. Для нахождения степени диссоциации гидроксида аммония можно воспользоваться математическим выражением закона разбавления Оствальда:
либо, опираясь на определение степени диссоциации, провести расчет на основании величин, полученных при решении закона действующих масс (степень диссоциации слабого электролита – это отношение количества распавшихся на ионы молекул к общему количеству растворенного вещества):
Ответ: α=1,33; [OH — ] = [ NH4 + ]=1,33∙10 -3 моль/л.
Слабые электролиты при растворении и расплавлении диссоциируют на ионы частично. Параллельно с процессом диссоциации идет обратный процесс – ассоциация – образование молекул из ионов. В определенный момент времени скорости прямой и обратной реакций выравниваются, и наступает состояние химического равновесия. В данном состоянии система будет находиться столь долго, пока какое-либо внешнее воздействие не приведет к смещению равновесия. Состояние химического равновесия характеризуется константой равновесия.
Выведем выражение для константы химического равновесия, опираясь на понятия химической кинетики.
1. Запишем уравнение диссоциации слабого электролита в общем виде:
2. Запишем уравнения для скорости прямой и обратной реакции через концентрации веществ:
3. Состояние химического равновесия характеризуется равенством скоростей прямой и обратной реакции:
4. Преобразуем последнее выражение, сгруппировав переменные величины (концентрации) в одной части выражения, а постоянные величины (константы скоростей) – в другой:
5. Так как отношение констант скоростей есть величина постоянная, вводим новую константу, которая будет характеризовать состояние химического равновесия.
6. На основании полученного выражения формулируем закон действующих масс. Для обратимой химической реакции в состоянии равновесия произведение равновесных концентраций продуктов реакции в степенях их стехиометрических коэффициентов, отнесенное к такому же произведению для исходных веществ, есть величина постоянная при данной температуре и давлении.
Константа химического равновесия есть величина постоянная при данной температуре и давлении; она не зависит от концентраций реагирующих веществ, а определяется лишь природой вещества и растворителя. Для слабых электролитов эта константа называется константой ионизации. Для сильных электролитов константа диссоциации не имеет смысла, так как данные вещества при растворении полностью диссоциируют на ионы.
Помимо константы ионизации силу электролита характеризует степень диссоциации. Степень диссоциации – это отношение числа распавшихся при диссоциации молекул на ионы, отнесенное к общему числу частиц растворенного вещества.

Между степенью диссоциации и константой ионизации существует математическая связь, выражаемая законом разбавления Оствальда:

если электролит слабый и степень диссоциации мала, то величиной α в знаменателе можно пренебречь по сравнению с единицей, в итоге получим упрощенное выражение закона разбавления Оствальда:
Закон разбавления Оствальда. При разбавлении слабого электролита степень его диссоциации увеличивается.
ido.tsu.ru
Скорость химической реакции
Говорить об осуществимости процесса можно по изменению энергии Гибсса системы. Но данная величина не отражает настоящую возможность протекания реакции, ее скорость и механизм.
Для полноценного представления химической реакции, надо иметь знания о том, какие существуют временные закономерности при ее осуществлении, т.е. скорость химической реакции и ее детальный механизм. Скорость и механизм реакции изучает химическая кинетика – наука о химическом процессе.
С точки зрения химической кинетики, реакции можно классифицировать на простые и сложные.
Простые реакции – процессы, протекающие без образования промежуточных соединений. По количеству частиц, принимающих в ней участие, они делятся на мономолекулярные, бимолекулярные, тримолекулярные. Соударение большего чем 3 числа частиц маловероятно, поэтому тримолекулярные реакции достаточно редки, а четырехмолекулярные — неизвестны. Сложные реакции – процессы, состоящие из нескольких элементарных реакций.
Любой процесс протекает с присущей ему скоростью, которую можно определить по изменениям, происходящим за некий отрезок времени. Среднюю скорость химической реакции выражают изменением количества вещества n израсходованного или полученного вещества в единице объема V за единицу времени t.
Если вещество расходуется, то ставим знак «-», если накапливается – «+»
При постоянном объеме:
Единица измерения скорости реакции моль/л·с
В целом, υ — величина постоянная и не зависит от того, за каким участвующим в реакции веществом, мы следим.
Зависимость концентрации реагента или продукта от времени протекания реакции представляют в виде кинетической кривой, которая имеет вид:
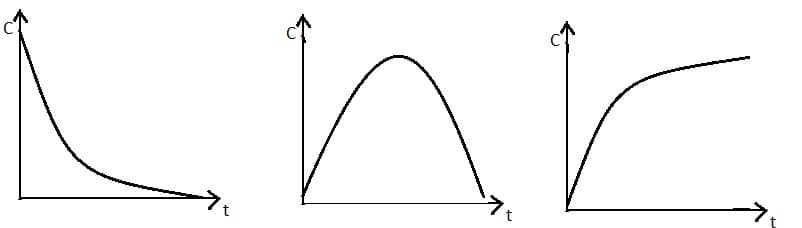
Вычислять υ из экспериментальных данных удобнее, если указанные выше выражения преобразовать в следующее выражение:

Закон действующих масс. Порядок и константа скорости реакции
Одна из формулировок закона действующих масс звучит следующим образом: Скорость элементарной гомогенной химической реакции прямо пропорциональна произведению концентраций реагентов.
Если исследуемый процесс представить в виде:
а А + b В = продукты
то скорость химической реакции можно выразить кинетическим уравнением:
а и b – стехиометрические коэффициенты простой реакции,
k – константа скорости реакции.
Химический смысл величины k — это скорость реакции при единичных концентрациях. То есть, если концентрации веществ А и В равны 1, то υ = k.
Надо учитывать, что в сложных химических процессах коэффициенты а и b не совпадают со стехиометрическими.
Закон действующих масс выполняется при соблюдении ряда условий:
- Реакция активируется термично, т.е. энергией теплового движения молекул.
- Концентрация реагентов распределена равномерно.
- Свойства и условия среды в ходе процесса не меняются.
- Свойства среды не должны влиять на k.
К сложным процессам закон действия масс применить нельзя. Это можно объяснить тем, что сложный процесс состоит из нескольких элементарных стадий, и его скорость будет определяться не суммарной скоростью всех стадий, лишь одной самой медленной стадией, которя называется лимитирующей.
Каждая реакция имеет свой порядок. Определяют частный (парциальный) порядок по реагенту и общий (полный) порядок. Например, в выражении скорости химической реакции для процесса
a – порядок по реагенту А
Для простых процессов порядок реакции указывает на количество реагирующих частиц (совпадает со стехиометрическими коэффициентами) и принимает целочисленные значения. Для сложных процессов порядок реакции не совпадает со стехиометрическими коэффициентами и может быть любым.
Определим факторы, влияющие на скорость химической реакции υ.
Зависимость скорости реакции от концентрации реагирующих веществ
Очевидно, что с увеличением концентраций реагирующих веществ, υ увеличивается, т.к. увеличивается число соударений между участвующими в химическом процессе веществами. Причем, важно учитывать порядок реакции: если это n = 1 по некоторому реагенту, то ее скорость прямо пропорциональна концентрации этого вещества. Если по какому-либо реагенту n = 2, то удвоение его концентрации приведет к росту скорости реакции в 2 2 = 4 раза, а увеличение концентрации в 3 раза ускорит реакцию в 3 2 = 9 раз.
Зависимость скорости реакции от давления
определяется уравнением Клапейрона – Менделеева, которое связывает концентрацию и давление:
Таким образом, изменение концентрации в системе, а следовательно и скорости реакции имеет прямую зависимость от изменения давления. Эта зависимость актуальна в первую очередь для процессов, идущих с участием газов. Например, для реакции первого порядка, увеличение давления в 2 раза вызовет рост концентрации вещества в 2 раза, что непременно изменит υ – она станет в 2 раза больше.
Зависимость скорости реакции от площади поверхности
касается гетерогенных реакций. Вещества реагируют быстрее, если площадь поверхности, на которой может происходить взаимодействие веществ больше. Растворяя вещество, мы уменьшаем его размеры до размеров молекулы, увеличивая тем самым площадь поверхности. Поэтому химические процессы между веществами, находящимися в растворенном, жидком или газообразном состоянии имеют большую скорость, чем взаимодействия между твердыми веществами.
Зависимость скорости реакции от природы вещества.
Имеет большое значение строение электронной оболочки атома, тип химической связи и ее прочность в молекулах, структура вещества, прочность его кристаллической решетки. Известно, что натрий будет активнее взаимодействовать с водой, чем, например, олово. Поэтому и скорость взаимодействия натрия с водой выше скорости взаимодействия олова с водой.
Зависимость скорости реакции от температуры
определяется правилом Вант-Гоффа и уравнением Аррениуса. Повышая температуру, мы сообщаем молекулам дополнительную энергию (увеличивая, тем самым, энергию активации), которая способствует протеканию реакции. Сванте Аррениус в 1889 году, изучая зависимость υ от температуры, установил, что большинство химических процессов подчиняются уравнению:
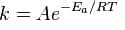
где k — константа скорости реакции
Еа -энергия активации – минимальная (критическая) энергия, необходимая для осуществления реакции, единица измерения Дж/моль
Т — абсолютная температура
R – газовая постоянная, R = 8,314 Дж/моль·град
A — предэкспоненциальный множитель (частотный фактор), единица измерения совпадает с k. Эта константа выражает вероятность того, что при столкновении молекулы будут ориентированы так, чтобы взаимодействие было возможно.
Часто бывает, что известна константа скорости при одной температуре Т1, а требуется найти k при некой другой температуре Т2. Это легко сделать, если взять логарифм уравнения Аррениуса при Т1 и Т2:
Вычитая второе равенство из первого, получаем:
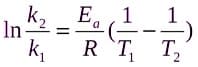
При определении скорости химической реакции, также можно использовать уравнение Аррениуса (в случае, если υ описывается степенным уравнением):
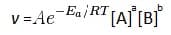
Если принять, что концентрации веществ А и В постоянны и прологарифмировать данное выражение, то получим следующее:
Также удобно пользоваться эмпирическим правилом, которое сформулировал Якоб Вант-Гофф: увеличение температуры на каждые 10 градусов, приводит к росту скорости реакции в 2 – 4 раза. Правило имеет математическое выражение:

γ — температурный коэффициент реакции, значения которого лежат в интервале от 2 до 4.
υT1/υT2 = 3 2 = 9. Это означает, что υ возросла в 9 раз.
Зависимость скорости реакции от присутствия катализатора
Катализ – это любое изменение скорости реакции под действием катализатора. Он может быть положительным и отрицательным. Суть катализа – генерирование активного субстрата или реагента с участием катализаторов.
Катализатор представляет собой вещество, которое селективно ускоряет химическую реакцию, вступая при этом в промежуточную стадию, но регенирируясь к ее концу (к моменту образования конечных продуктов). Например, в биохимической среде в качестве катализаторов выступают ферменты.
Если такое вещество замедляет химическую реакцию, то оно называется ингибитором.
Влияние катализатора на скорость реакции основывается на том, что он изменяет энергию активации Еа или А. Понижение энергии активации под действием катализатора схематично представлено на рисунке ниже:
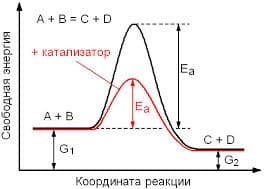 влияние катализатора на энергию активации
влияние катализатора на энергию активации
Видно, что веществам А и В требуется большое количество энергии, чтобы образовать конечные продукты. Но в присутствии катализатора для получения конечных продуктов требуется гораздо меньше энергии, т.к. идет понижение полной энергии активации, и тем самым, увеличение скорости реакции. Обращаю ваше внимание на то, что энергии как начальных, так и конечных веществ остаются одинаковыми в обеих реакциях.
zadachi-po-khimii.ru
